ალკენები ქიმიურად აქტიურია. მათი ქიმიური თვისებები დიდწილად განისაზღვრება ორმაგი ბმის არსებობით. ალკენების ყველაზე გავრცელებული რეაქციებია ელექტროფილური დამატების და რადიკალური დამატების რეაქციები. ნუკლეოფილური დამატების რეაქციები ჩვეულებრივ მოითხოვს ძლიერი ნუკლეოფილის არსებობას და არ არის დამახასიათებელი ალკენებისთვის. ალკენები ადვილად განიცდიან ჟანგვის და დამატების რეაქციებს და ასევე შეუძლიათ ალილის რადიკალების ჩანაცვლება.
დანამატის რეაქციები
ჰიდროგენიზაცია წყალბადის დამატება (ჰიდროგენაციის რეაქცია) ალკენებში ხდება კატალიზატორების თანდასწრებით. ყველაზე ხშირად გამოიყენება დაქუცმაცებული ლითონები - პლატინა, ნიკელი, პალადიუმი და ა.შ. შედეგად წარმოიქმნება შესაბამისი ალკანები (გაჯერებული ნახშირწყალბადები).
$CH_2=CH_2 + H2 → CH_3–CH_3$
ჰალოგენების დამატება. ალკენები ადვილად, ჩვეულებრივ პირობებში, რეაგირებენ ქლორთან და ბრომთან და წარმოქმნიან შესაბამის დიჰალოალკანებს, რომლებშიც ჰალოგენის ატომები განლაგებულია ნახშირბადის ატომების მიმდებარედ.
შენიშვნა 1
როდესაც ალკენები ბრომთან ურთიერთქმედებენ, ბრომი უფერულდება ყვითელ-ყავისფერ ფერამდე. ეს არის ერთ-ერთი უძველესი და უმარტივესი ხარისხობრივი რეაქცია უჯერი ნახშირწყალბადებისთვის, ვინაიდან ალკინები და ალკადიენებიც ანალოგიურად რეაგირებენ.
$CH_2=CH_2 + Br_2 → CH_2Br–CH_2Br$
წყალბადის ჰალოიდების დამატება. როდესაც ეთილენის ნახშირწყალბადები რეაგირებენ წყალბადის ჰალოგენებთან ($HCl$, $HBr$), წარმოიქმნება ჰალოალკანები; რეაქციის მიმართულება დამოკიდებულია ალკენების სტრუქტურაზე.
ეთილენის ან სიმეტრიული ალკენების შემთხვევაში, დამატების რეაქცია ხდება ცალსახად და იწვევს მხოლოდ ერთი პროდუქტის წარმოქმნას:
$CH_2=CH_2 + HBr → CH_3–CH_2Br$
არასიმეტრიული ალკენების შემთხვევაში შესაძლებელია ორი განსხვავებული დამატების რეაქციის პროდუქტის წარმოქმნა:
შენიშვნა 2
სინამდვილეში, ძირითადად მხოლოდ ერთი რეაქციის პროდუქტი იქმნება. ნიმუში ასეთი რეაქციების მიმართულებით დაადგინა რუსმა ქიმიკოსმა ვ.ვ. მარკოვნიკოვი 1869 წელს მას უწოდებენ მარკოვნიკოვის მმართველობას. როდესაც წყალბადის ჰალოგენები რეაგირებენ არასიმეტრიულ ალკენებთან, წყალბადის ატომი ემატება ორმაგი ბმის გაწყვეტის ადგილზე ყველაზე წყალბადირებულ ნახშირბადის ატომზე, ანუ მანამ, სანამ იგი დაუკავშირდება წყალბადის ატომების დიდ რაოდენობას.
მარკოვნიკოვმა ეს წესი ექსპერიმენტული მონაცემების საფუძველზე ჩამოაყალიბა და მხოლოდ გაცილებით მოგვიანებით მიიღო თეორიული დასაბუთება. განვიხილოთ პროპილენის რეაქცია წყალბადის ქლორიდთან.
$p$ ბონდის ერთ-ერთი მახასიათებელია მისი ადვილად პოლარიზების უნარი. პროპენის მოლეკულაში მეთილის ჯგუფის (დადებითი ინდუქციური ეფექტი + $I$) გავლენით, $p$ ბმის ელექტრონის სიმკვრივე გადადის ნახშირბადის ერთ-ერთ ატომზე (= $CH_2$). შედეგად, მასზე ჩნდება ნაწილობრივი უარყოფითი მუხტი ($\delta -$). ნაწილობრივი დადებითი მუხტი ($\delta +$) ჩნდება ორმაგი ბმის სხვა ნახშირბადის ატომზე.
პროპილენის მოლეკულაში ელექტრონის სიმკვრივის ეს განაწილება განსაზღვრავს მომავალი პროტონის შეტევის ადგილს. ეს არის მეთილენის ჯგუფის ნახშირბადის ატომი (= $CH_2$), რომელიც ატარებს ნაწილობრივ უარყოფით $\delta-$ მუხტს. და ქლორი, შესაბამისად, უტევს ნახშირბადის ატომს ნაწილობრივი დადებითი მუხტით $\დელტა+$.
შედეგად, პროპილენის რეაქციის ძირითადი პროდუქტი წყალბადის ქლორიდთან არის 2-ქლოროპროპანი.
დატენიანება
ალკენების ჰიდრატაცია ხდება მინერალური მჟავების თანდასწრებით და ემორჩილება მარკოვნიკოვის წესს. რეაქციის პროდუქტებია ალკოჰოლი
$CH_2=CH_2 + H_2O → CH_3–CH_2–OH$
ალკილაცია
ალკანების დამატება ალკენებში მჟავა კატალიზატორის ($HF$ ან $H_2SO_4$) თანდასწრებით დაბალ ტემპერატურაზე იწვევს ნახშირწყალბადების უფრო მაღალი მოლეკულური წონის წარმოქმნას და ხშირად გამოიყენება ინდუსტრიაში საავტომობილო საწვავის წარმოებისთვის.
$R–CH_2=CH_2 + R’–H → R–CH_2–CH_2–R’$
ჟანგვის რეაქციები
ალკენების დაჟანგვა შეიძლება მოხდეს ჟანგვის რეაგენტების პირობებისა და ტიპების მიხედვით, როგორც ორმაგი ბმის გაწყვეტით, ასევე ნახშირბადის ჩონჩხის შენარჩუნებით:
პოლიმერიზაციის რეაქციები
ალკენის მოლეკულებს შეუძლიათ გარკვეულ პირობებში დაემატონ ერთმანეთს $\pi$ ბმების გახსნით და დიმერების, ტრიმერების ან მაღალი მოლეკულური წონის ნაერთების - პოლიმერების წარმოქმნით. ალკენების პოლიმერიზაცია შეიძლება მოხდეს როგორც თავისუფალი რადიკალით, ასევე კათიონ-ანიონის მექანიზმით. პოლიმერიზაციის ინიციატორებად გამოიყენება მჟავები, პეროქსიდები, ლითონები და ა.შ.პოლიმერიზაციის რეაქციაც მიმდინარეობს ტემპერატურის, დასხივების, წნევის გავლენით. ტიპიური მაგალითია ეთილენის პოლიმერიზაცია პოლიეთილენის წარმოქმნით
$nCH_2=CH_2 → (–CH_2–CH_(2^–))_n$
ჩანაცვლების რეაქციები
ჩანაცვლების რეაქციები არ არის დამახასიათებელი ალკენებისთვის. თუმცა, მაღალ ტემპერატურაზე (400 ° C-ზე მეტი), რადიკალური დამატების რეაქციები, რომლებიც შექცევადია, ჩახშობილია. ამ შემთხვევაში შესაძლებელი ხდება წყალბადის ატომის შეცვლა, რომელიც მდებარეობს ალილურ მდგომარეობაში ორმაგი კავშირის შენარჩუნებით.
$CH_2=CH–CH_3 + Cl_2 – CH_2=CH–CH_2Cl + HCl$
ცოდნის ჰიპერმარკეტი >>ქიმია >>ქიმია მე-10 კლასი >> ქიმია: ალკენები
უჯერი მოიცავს ნახშირწყალბადებს, რომლებიც შეიცავს მრავალ კავშირს ნახშირბადის ატომებს შორის მათ მოლეკულებში. უჯერია ალკენები, ალკინები, ალკადიენები (პოლიენები). უჯერი ხასიათი აქვთ აგრეთვე ციკლურ ნახშირწყალბადებს, რომლებიც შეიცავს ორმაგ ბმას რგოლში (ციკლოალკენები), ისევე როგორც ციკლოალკანებს რგოლში ნახშირბადის ატომების მცირე რაოდენობით (სამი ან ოთხი ატომით). "გაუჯერებლობის" თვისება დაკავშირებულია ამ ნივთიერებების უნართან, შევიდნენ დამატებით რეაქციებში, პირველ რიგში წყალბადში, გაჯერებული ან გაჯერებული ნახშირწყალბადების - ალკანების წარმოქმნით.
სტრუქტურა
ალკენები აციკლურია, მოლეკულაში, ცალკეული ბმების გარდა, შეიცავს ერთ ორმაგ კავშირს ნახშირბადის ატომებს შორის და შეესაბამება ზოგად ფორმულას C n H 2n.
ალკენებმა მიიღეს მეორე სახელი - "ოლეფინები" უჯერი ცხიმოვანი მჟავების ანალოგიით (ოლეინი, ლინოლეური), რომელთა ნარჩენები თხევადი ცხიმების ნაწილია - ზეთები (ინგლისური ზეთიდან - ზეთი).
ნახშირბადის ატომები, რომლებსაც აქვთ ორმაგი ბმა მათ შორის, როგორც მოგეხსენებათ, იმყოფებიან sp 2 ჰიბრიდიზაციის მდგომარეობაში. ეს ნიშნავს, რომ ერთი s და ორი p ორბიტალი ჩართულია ჰიბრიდიზაციაში, ხოლო ერთი p ორბიტალი რჩება არაჰიბრიდირებული. ჰიბრიდული ორბიტალების გადახურვა იწვევს a-ბმას, ხოლო ეთილენის მოლეკულის მეზობელი ნახშირბადის ატომების არაჰიბრიდირებული ორბიტალების გამო წარმოიქმნება მეორე, პ- კავშირი. ამრიგად, ორმაგი ბმა შედგება ერთი Þ-ბმა და ერთი p-ბმა.
ორმაგი ბმის შემქმნელი ატომების ჰიბრიდული ორბიტალები იმავე სიბრტყეშია, ხოლო ორბიტალები, რომლებიც ქმნიან n-ბმას, განლაგებულია მოლეკულის სიბრტყის პერპენდიკულარულად (იხ. სურ. 5).
ორმაგი ბმა (0,132 ნმ) უფრო მოკლეა, ვიდრე ერთი ბმა და მისი ენერგია უფრო მაღალია, ანუ უფრო ძლიერია. მიუხედავად ამისა, მობილური, ადვილად პოლარიზებადი 7გ ბმის არსებობა იწვევს იმ ფაქტს, რომ ალკენები ქიმიურად უფრო აქტიურია ვიდრე ალკანები და შეუძლიათ განიცადონ დამატების რეაქციები.
ეთენის ჰომოლოგიური სერია
სწორი ჯაჭვის ალკენები ქმნიან ეთენის (ეთილენის) ჰომოლოგიურ სერიას.
C2H4 - ეთენი, C3H6 - პროპენი, C4H8 - ბუტენი, C5H10 - პენტენი, C6H12 - ჰექსენი და ა.შ.
იზომერიზმი და ნომენკლატურა
ალკენებს, ისევე როგორც ალკანებს, ახასიათებთ სტრუქტურული იზომერიზმი. სტრუქტურული იზომერები, როგორც გახსოვთ, განსხვავდება ერთმანეთისგან ნახშირბადის ჩონჩხის აგებულებით. უმარტივესი ალკენი, რომელიც ხასიათდება სტრუქტურული იზომერებით, არის ბუტენი.
CH3-CH2-CH=CH2 CH3-C=CH2
ლ
CH3
ბუტენი-1 მეთილპროპენი
სტრუქტურული იზომერიზმის განსაკუთრებული ტიპია ორმაგი ბმის პოზიციის იზომერიზმი:
CH3-CH2-CH=CH2 CH3-CH=CH-CH3
ბუტენი-1 ბუტენ-2
ნახშირბადის ატომების თითქმის თავისუფალი ბრუნვა შესაძლებელია ერთი ნახშირბად-ნახშირბადის ბმის გარშემო, ამიტომ ალკანის მოლეკულებს შეუძლიათ მიიღონ მრავალფეროვანი ფორმები. ორმაგი ბმის ირგვლივ ბრუნვა შეუძლებელია, რაც იწვევს ალკენებში იზომერიზმის სხვა სახეობის - გეომეტრიულ, ან ცის-ტრანს იზომერიზმი.
ცის იზომერები განსხვავდებიან გულმკერდის იზომერებისგან მოლეკულური ფრაგმენტების (ამ შემთხვევაში, მეთილის ჯგუფების) სივრცითი განლაგებით სიბრტყესთან მიმართებაში. პ- კავშირები და, შესაბამისად, თვისებები.
ალკენები იზომერულია ციკლოალკანებთან (კლასთაშორისი იზომერიზმი), მაგალითად:
CH2 = CH-CH2-CH2-CH2-CH3
ჰექსენი-1 ციკლოჰექსანი
ნომენკლატურა ალკენები IUPAC-ის მიერ შემუშავებული, მსგავსია ალკანების ნომენკლატურის.
1. მთავარი წრედის შერჩევა
ნახშირწყალბადის სახელის ფორმირება იწყება ძირითადი ჯაჭვის განსაზღვრით - ნახშირბადის ატომების ყველაზე გრძელი ჯაჭვი მოლეკულაში. ალკენების შემთხვევაში, მთავარი ჯაჭვი უნდა შეიცავდეს ორმაგ ბმას.
2. ძირითადი ჯაჭვის ატომების ნუმერაცია
მთავარი ჯაჭვის ატომების ნუმერაცია იწყება იმ ბოლოდან, რომელთანაც ორმაგი ბმა არის ყველაზე ახლოს. მაგალითად, სწორი კავშირის სახელია
dn3-dn-dn2-dn=dn-dn3 dn3
5-მეთილჰექსენ-2 და არა 2-მეთილჰექსენ-4, როგორც შეიძლება ველოდოთ.
თუ ორმაგი ბმის პოზიცია ვერ განსაზღვრავს ჯაჭვში ატომების ნუმერაციის დასაწყისს, მაშინ იგი განისაზღვრება შემცვლელების პოზიციით ისევე, როგორც გაჯერებული ნახშირწყალბადებისთვის.
CH3- CH2-CH=CH-CH-CH3
ლ
CH3
2-მეთილჰექსენი-3
3. სახელწოდების ფორმირება
ალკენების სახელები იქმნება ისევე, როგორც ალკანების სახელები. სახელის ბოლოს მიუთითეთ ნახშირბადის ატომის რაოდენობა, რომლიდანაც იწყება ორმაგი ბმა და სუფიქსი, რომელიც მიუთითებს, რომ ნაერთი მიეკუთვნება ალკენების კლასს -ენი.
ქვითარი
1. ნავთობპროდუქტების კრეკინგი. გაჯერებული ნახშირწყალბადების თერმული კრეკინგის პროცესში, ალკანების წარმოქმნასთან ერთად, ხდება ალკენების წარმოქმნა.
2. გაჯერებული ნახშირწყალბადების დეჰიდროგენაცია. როდესაც ალკანები გადადიან კატალიზატორზე მაღალ ტემპერატურაზე (400-600 °C), წყალბადის მოლეკულა გამოიყოფა და წარმოიქმნება ალკენი: 
3. სპირტების დეჰიდრატაცია (წყლის ელიმინაცია). წყლის გამწმენდი საშუალებების (H2804, Al203) ეფექტი მონოჰიდრულ სპირტებზე მაღალ ტემპერატურაზე იწვევს წყლის მოლეკულის აღმოფხვრას და ორმაგი ბმის წარმოქმნას:
ამ რეაქციას ეწოდება ინტრამოლეკულური დეჰიდრატაცია (ინტრამოლეკულური დეჰიდრატაციისგან განსხვავებით, რომელიც იწვევს ეთერების წარმოქმნას და შესწავლილი იქნება § 16 „ალკოჰოლები“).
4. დეჰიდროჰალოგენაცია (წყალბადის ჰალოგენის ელიმინაცია).
როდესაც ჰალოალკანი რეაგირებს ტუტესთან სპირტის ხსნარში, წყალბადის ჰალოგენის მოლეკულის ელიმინაციის შედეგად წარმოიქმნება ორმაგი ბმა.
გაითვალისწინეთ, რომ ეს რეაქცია წარმოქმნის უპირატესად ბუტენ-2-ს და არა ბუტენ-1-ს, რაც შეესაბამება ზაიცევის წესი:
როდესაც წყალბადის ჰალოიდი გამოიყოფა მეორადი და მესამეული ჰალოალკანებიდან, წყალბადის ატომი გამოიყოფა ყველაზე ნაკლებად ჰიდროგენირებული ნახშირბადის ატომიდან.
5. დეჰალოგენაცია. როდესაც თუთია მოქმედებს ალკანის დიბრომო წარმოებულზე, მეზობელ ნახშირბადის ატომებზე მდებარე ჰალოგენის ატომები აღმოიფხვრება და იქმნება ორმაგი ბმა: 
ფიზიკური თვისებები
ალკენების ჰომოლოგიური სერიის პირველი სამი წარმომადგენელია აირები, C5H10-C16H32 შემადგენლობის ნივთიერებები სითხეებია, უმაღლესი ალკენები კი მყარი.
დუღილის და დნობის წერტილები ბუნებრივად იზრდება ნაერთების მოლეკულური წონის მატებასთან ერთად.
ქიმიური თვისებები
დანამატის რეაქციები
შეგახსენებთ, რომ უჯერი ნახშირწყალბადების - ალკენების წარმომადგენლების გამორჩეული თვისებაა დამატების რეაქციებში შესვლის უნარი. ამ რეაქციების უმეტესობა მიმდინარეობს ელექტროფილური დამატების მექანიზმით.
1. ალკენების ჰიდროგენიზაცია. ალკენებს შეუძლიათ წყალბადის დამატება ჰიდროგენიზაციის კატალიზატორების - ლითონების - პლატინის, პალადიუმის, ნიკელის თანდასწრებით:
CH3-CH2-CH=CH2 + H2 -> CH3-CH2-CH2-CH3
ეს რეაქცია ხდება როგორც ატმოსფერულ, ასევე ამაღლებულ წნევაზე და არ საჭიროებს მაღალ ტემპერატურას, რადგან ის ეგზოთერმულია. როდესაც ტემპერატურა იზრდება, იგივე კატალიზატორებმა შეიძლება გამოიწვიოს საპირისპირო რეაქცია - დეჰიდროგენაცია.
2. ჰალოგენაცია (ჰალოგენების დამატება). ალკენის ურთიერთქმედება ბრომიან წყალთან ან ბრომის ხსნართან ორგანულ გამხსნელში (CCl4) იწვევს ამ ხსნარების სწრაფ გაუფერულებას ალკენში ჰალოგენის მოლეკულის დამატების და დიჰალოალკანების წარმოქმნის შედეგად.
მარკოვნიკოვი ვლადიმერ ვასილიევიჩი
(1837-1904)
რუსი ორგანული ქიმიკოსი. ჩამოაყალიბა (1869) წესები ჩანაცვლების მიმართულების, აღმოფხვრის, ორმაგი ბმის დროს დამატებისა და იზომერიზაციის რეაქციების შესახებ, რაც დამოკიდებულია ქიმიურ სტრუქტურაზე. შეისწავლა (1880 წლიდან) ნავთობის შემადგენლობა და საფუძველი ჩაუყარა ნავთობქიმიას, როგორც დამოუკიდებელ მეცნიერებას. აღმოაჩინა (1883) ორგანული ნივთიერებების ახალი კლასი - ციკლო-პარაფინები (ნაფთენები).
3. ჰიდროჰალოგენაცია (წყალბადის ჰალოგენის დამატება).
წყალბადის ჰალოგენური დამატების რეაქცია უფრო დეტალურად იქნება განხილული ქვემოთ. ეს რეაქცია ემორჩილება მარკოვნიკოვის წესს:
როდესაც წყალბადის ჰალოგენი მიმაგრებულია ალკენს, წყალბადი ემაგრება უფრო წყალბადირებულ ნახშირბადის ატომს, ანუ ატომს, რომელშიც მეტი წყალბადის ატომია, ხოლო ჰალოგენი ნაკლებად წყალბადის ატომს.
4. დატენიანება (წყლის დამატება). ალკენების დატენიანება იწვევს ალკოჰოლების წარმოქმნას. მაგალითად, ეთენში წყლის დამატება საფუძვლად უდევს ეთილის სპირტის წარმოების ერთ-ერთ სამრეწველო მეთოდს:
CH2=CH2 + H2O -> CH3-CH2OH
ეთენის ეთანოლი
გაითვალისწინეთ, რომ პირველადი ალკოჰოლი (პირველ ნახშირბადზე ჰიდროქსი ჯგუფით) წარმოიქმნება მხოლოდ მაშინ, როდესაც ეთენი ჰიდრატირებულია. პროპენის ან სხვა ალკენების ჰიდრატაციისას წარმოიქმნება მეორადი სპირტები. 
ეს რეაქციაც მარკოვნიკოვის წესით მიმდინარეობს - წყალბადის კატიონი უერთდება უფრო ჰიდროგენიზებულ ნახშირბადის ატომს, ხოლო ჰიდროქსი ჯგუფი - ნაკლებად ჰიდროგენიზებულს.
5. პოლიმერიზაცია. დამატების განსაკუთრებული შემთხვევაა ალკენების პოლიმერიზაციის რეაქცია:
ეს დამატების რეაქცია ხდება თავისუფალი რადიკალების მექანიზმის მეშვეობით.
ჟანგვის რეაქციები
ნებისმიერი ორგანული ნაერთების მსგავსად, ალკენები იწვის ჟანგბადში CO2 და H20 წარმოქმნით.
ალკანებისგან განსხვავებით, რომლებიც მდგრადია ხსნარებში დაჟანგვის მიმართ, ალკენები ადვილად იჟანგება კალიუმის პერმანგანატის წყალხსნარების მოქმედებით. ნეიტრალურ ან ოდნავ ტუტე ხსნარებში ხდება ალკენების დაჟანგვა დიოლებამდე (დიჰიდრული სპირტები) და ჰიდროქსილის ჯგუფები ემატება იმ ატომებს, რომელთა შორის ორმაგი ბმა არსებობდა დაჟანგამდე.
როგორც უკვე იცით, უჯერი ნახშირწყალბადებს - ალკენებს შეუძლიათ შევიდნენ დამატებით რეაქციებში. ამ რეაქციების უმეტესობა მიმდინარეობს ელექტროფილური დამატების მექანიზმით.
ელექტროფილური კავშირი
ელექტროფილური რეაქციები არის რეაქციები, რომლებიც წარმოიქმნება ელექტროფილების გავლენის ქვეშ - ნაწილაკების, რომლებსაც აქვთ ელექტრონის სიმკვრივის ნაკლებობა, მაგალითად, შეუვსებელი ორბიტალი. უმარტივესი ელექტროფილური ნაწილაკი არის წყალბადის კატიონი. ცნობილია, რომ წყალბადის ატომს აქვს ერთი ელექტრონი მე-3 ორბიტალში. წყალბადის კატიონი წარმოიქმნება, როდესაც ატომი კარგავს ამ ელექტრონს, ამიტომ წყალბადის კატიონს საერთოდ არ აქვს ელექტრონები:
Н· - 1е - -> Н +
ამ შემთხვევაში, კატიონს აქვს საკმაოდ მაღალი ელექტრონის აფინურობა. ამ ფაქტორების ერთობლიობა წყალბადის კატიონს საკმაოდ ძლიერ ელექტროფილურ ნაწილაკად აქცევს.
წყალბადის კათიონის წარმოქმნა შესაძლებელია მჟავების ელექტროლიტური დისოციაციის დროს:
НВr -> Н + + Вr -
სწორედ ამ მიზეზით ხდება მრავალი ელექტროფილური რეაქცია მჟავების თანდასწრებითა და მონაწილეობით.
ელექტროფილური ნაწილაკები, როგორც უკვე აღვნიშნეთ, მოქმედებენ სისტემებზე, რომლებიც შეიცავს გაზრდილი ელექტრონის სიმკვრივის უბნებს. ასეთი სისტემის მაგალითია ნახშირბადის ნახშირბადის მრავალჯერადი (ორმაგი ან სამმაგი) ბმა.
თქვენ უკვე იცით, რომ ნახშირბადის ატომები, რომელთა შორის ორმაგი ბმა იქმნება, sp 2 ჰიბრიდიზაციის მდგომარეობაში არიან. იმავე სიბრტყეში განლაგებული მეზობელი ნახშირბადის ატომების არაჰიბრიდირებული p-ორბიტალების გადახურვა და ფორმირება პ-ბმა, რომელიც ნაკლებად ძლიერია ვიდრე Þ-ბმა და, რაც მთავარია, ადვილად პოლარიზდება გარე ელექტრული ველის გავლენით. ეს ნიშნავს, რომ დადებითად დამუხტული ნაწილაკის მიახლოებისას CS ბმის ელექტრონები გადაინაცვლებს მისკენ და ე.წ. P-კომპლექსი.
თურმე პ- კომპლექსური და წყალბადის კათიონის დამატების შემდეგ პ- კავშირები. წყალბადის კატიონი, როგორც ჩანს, ეჯახება მოლეკულის სიბრტყიდან ამოსულ ელექტრონის სიმკვრივეს პ- დაკავშირება და უერთდება. ![]()
შემდეგ ეტაპზე ხდება ელექტრონული წყვილის სრული გადაადგილება პ-ბმა ნახშირბადის ერთ-ერთ ატომთან, რაც იწვევს მასზე ელექტრონების მარტოხელა წყვილის გამოჩენას. ნახშირბადის ატომის ორბიტალი, რომელზედაც ეს წყვილი მდებარეობს და წყალბადის კატიონის დაუკავებელი ორბიტალი გადახურულია, რაც იწვევს კოვალენტური ბმის წარმოქმნას დონორ-მიმღები მექანიზმის მეშვეობით. ნახშირბადის მეორე ატომს ჯერ კიდევ აქვს შეუვსებელი ორბიტალი, ანუ დადებითი მუხტი.
მიღებულ ნაწილაკს კარბოკატიონი ეწოდება, რადგან ნახშირბადის ატომზე დადებით მუხტს შეიცავს. ამ ნაწილაკს შეუძლია გაერთიანდეს ნებისმიერ ანიონთან, ნაწილაკთან, რომელსაც აქვს მარტოხელა ელექტრონული წყვილი, ანუ ნუკლეოფილი.
მოდით განვიხილოთ ელექტროფილური დანამატის რეაქციის მექანიზმი ეთენის ჰიდრობრომაციის (წყალბადის ბრომიდის დამატება) მაგალითის გამოყენებით:
СН2= СН2 + НВг --> СНВr-СН3
რეაქცია იწყება ელექტროფილური ნაწილაკის – წყალბადის კატიონის წარმოქმნით, რომელიც წარმოიქმნება ბრომიდის წყალბადის მოლეკულის დისოციაციის შედეგად.
წყალბადის კათიონის შეტევები პ- კავშირი, ფორმირება პ- კომპლექსი, რომელიც სწრაფად გარდაიქმნება კარბოკაციონად: 
ახლა მოდით შევხედოთ უფრო რთულ შემთხვევას.
ეთენში წყალბადის ბრომიდის დამატების რეაქცია ცალსახად მიმდინარეობს და წყალბადის ბრომიდის ურთიერთქმედება პროპენთან თეორიულად შეიძლება მივიღოთ ორი პროდუქტი: 1-ბრომოპროპანი და 2-ბრომოპროპანი. ექსპერიმენტული მონაცემები აჩვენებს, რომ ძირითადად იწარმოება 2-ბრომოპროპანი.
ამის ასახსნელად მოგვიწევს გავითვალისწინოთ შუალედური ნაწილაკი - კარბოკატიონი.
პროპენში წყალბადის კატიონის დამატებამ შეიძლება გამოიწვიოს ორი კარბოკატიონის წარმოქმნა: თუ წყალბადის კატიონი შეუერთდება ნახშირბადის პირველ ატომს, ჯაჭვის ბოლოში მდებარე ატომს, მაშინ მეორეს ექნება დადებითი მუხტი, ე.ი. მოლეკულის ცენტრი (1); თუ ის შეუერთდება მეორეს, მაშინ პირველ ატომს ექნება დადებითი მუხტი (2). 
რეაქციის უპირატესი მიმართულება დამოკიდებული იქნება იმაზე, თუ რომელი კარბოკატიონი არის უფრო უხვი რეაქციის გარემოში, რაც, თავის მხრივ, განისაზღვრება კარბოკატიონის სტაბილურობით. ექსპერიმენტი აჩვენებს 2-ბრომოპროპანის უპირატესად წარმოქმნას. ეს ნიშნავს, რომ კარბოკატიონის (1) ფორმირება დადებითი მუხტით ცენტრალურ ატომზე უფრო დიდი რაოდენობით ხდება.
ამ კარბოკატიონის უფრო დიდი სტაბილურობა აიხსნება იმით, რომ ნახშირბადის ცენტრალურ ატომზე დადებითი მუხტი კომპენსირდება ორი მეთილის ჯგუფის დადებითი ინდუქციური ეფექტით, რომელთა საერთო ეფექტი უფრო მაღალია, ვიდრე ერთი ეთილის ჯგუფის +/- ეფექტი:
ალკენების ჰიდროჰალოგენიზაციის რეაქციების კანონები შეისწავლა ცნობილმა რუსმა ქიმიკოსმა V.V. Markovnikov-მა, A.M. Butlerov-ის სტუდენტმა, რომელმაც, როგორც ზემოთ აღინიშნა, ჩამოაყალიბა წესი, რომელიც ატარებს მის სახელს.
ეს წესი დამკვიდრდა ემპირიულად, ანუ ექსპერიმენტულად. ამჟამად ჩვენ შეგვიძლია მივცეთ სრულიად დამაჯერებელი ახსნა.
საინტერესოა, რომ სხვა ელექტროფილური დამატების რეაქციები ასევე ემორჩილება მარკოვნიკოვის წესს, ამიტომ სწორი იქნებოდა მისი უფრო ზოგადი ფორმით ჩამოყალიბება.
ელექტროფილური დამატების რეაქციებში ელექტროფილი (ნაწილაკი შეუვსებელი ორბიტალით) ემატება უფრო ჰიდროგენიზებულ ნახშირბადის ატომს, ხოლო ნუკლეოფილი (ნაწილაკი მარტოხელა წყვილი ელექტრონებით) ემატება ნაკლებად ჰიდროგენიზებულს.
პოლიმერიზაცია
დამატების რეაქციის განსაკუთრებული შემთხვევაა ალკენების და მათი წარმოებულების პოლიმერიზაციის რეაქცია. ეს რეაქცია მიმდინარეობს თავისუფალი რადიკალების დამატების მექანიზმით:
პოლიმერიზაცია ხორციელდება ინიციატორების - პეროქსიდის ნაერთების თანდასწრებით, რომლებიც წარმოადგენენ თავისუფალი რადიკალების წყაროს. პეროქსიდის ნაერთები არის ნივთიერებები, რომელთა მოლეკულები მოიცავს -O-O- ჯგუფს. პეროქსიდის უმარტივესი ნაერთია წყალბადის ზეჟანგი HOOH.
100 °C ტემპერატურაზე და 100 მპა წნევაზე ხდება არასტაბილური ჟანგბად-ჟანგბადის ბმის ჰომოლიზი და წარმოიქმნება რადიკალები - პოლიმერიზაციის ინიციატორები. KO- რადიკალების გავლენით იწყება პოლიმერიზაცია, რომელიც ვითარდება თავისუფალი რადიკალების დამატების რეაქციის სახით. ჯაჭვის ზრდა ჩერდება, როდესაც რეაქციის ნარევში ხდება რადიკალების რეკომბინაცია - პოლიმერული ჯაჭვი და რადიკალები ან COCH2CH2-.
ორმაგი ბმის შემცველი ნივთიერებების თავისუფალი რადიკალების პოლიმერიზაციის რეაქციის გამოყენებით, მიიღება დიდი რაოდენობით მაღალი მოლეკულური წონის ნაერთები: 
ალკენების გამოყენება სხვადასხვა შემცვლელებთან ერთად შესაძლებელს ხდის პოლიმერული მასალების ფართო სპექტრის სინთეზირებას, თვისებების ფართო სპექტრით. 
ყველა ეს პოლიმერული ნაერთი ფართოდ გამოიყენება ადამიანის საქმიანობის სხვადასხვა სფეროში - მრეწველობა, მედიცინა, გამოიყენება ბიოქიმიური ლაბორატორიების აღჭურვილობის წარმოებისთვის, ზოგი შუალედურია სხვა მაღალმოლეკულური ნაერთების სინთეზისთვის.
ოქსიდაცია
თქვენ უკვე იცით, რომ ნეიტრალურ ან ოდნავ ტუტე ხსნარებში ხდება ალკენების დაჟანგვა დიოლებამდე (დიჰიდრული სპირტები). მჟავე გარემოში (გოგირდის მჟავით დამჟავებული ხსნარი) ორმაგი ბმა მთლიანად განადგურებულია და ნახშირბადის ატომები, რომელთა შორის ორმაგი ბმა არსებობდა, გარდაიქმნება კარბოქსილის ჯგუფის ნახშირბადის ატომებად: 
ალკენების დესტრუქციული დაჟანგვა შეიძლება გამოყენებულ იქნას მათი სტრუქტურის დასადგენად. მაგალითად, თუ ძმარმჟავა და პროპიონის მჟავები მიიღება გარკვეული ალკენის დაჟანგვის დროს, ეს ნიშნავს, რომ პენტენ-2 განიცადა დაჟანგვა, ხოლო თუ მიიღება ბუტირის მჟავა და ნახშირორჟანგი, მაშინ ორიგინალური ნახშირწყალბადი არის პენტენ-1. .
განაცხადი
ალკენები ფართოდ გამოიყენება ქიმიურ მრეწველობაში, როგორც ნედლეული სხვადასხვა ორგანული ნივთიერებებისა და მასალების წარმოებისთვის.
მაგალითად, ეთენი არის საწყისი მასალა ეთანოლის, ეთილენგლიკოლის, ეპოქსიდების და დიქლოროეთანის წარმოებისთვის.
დიდი რაოდენობით ეთენი მუშავდება პოლიეთილენად, რომელიც გამოიყენება შესაფუთი ფირის, ჭურჭლის, მილების და ელექტროსაიზოლაციო მასალების დასამზადებლად.
პროპენისგან მიიღება გლიცერინი, აცეტონი, იზოპროპანოლი და გამხსნელები. პროპენის პოლიმერიზაციით მიიღება პოლიპროპილენი, რომელიც მრავალი თვალსაზრისით აღემატება პოლიეთილენს: მას აქვს უფრო მაღალი დნობის წერტილი და ქიმიური წინააღმდეგობა.
ამჟამად უნიკალური თვისებების მქონე ბოჭკოები იწარმოება პოლიმერებისგან - პოლიეთილენის ანალოგებისგან. მაგალითად, პოლიპროპილენის ბოჭკო უფრო ძლიერია ვიდრე ყველა ცნობილი სინთეზური ბოჭკო.
ამ ბოჭკოებისგან დამზადებული მასალები პერსპექტიულია და სულ უფრო ხშირად გამოიყენება ადამიანის საქმიანობის სხვადასხვა სფეროში.

1. რა სახის იზომერიზმია დამახასიათებელი ალკენებისთვის? დაწერეთ პენტენ-1-ის შესაძლო იზომერების ფორმულები.
2. რა ნაერთებიდან შეიძლება მივიღოთ: ა) იზობუტენი (2-მეთილპროპენი); ბ) ბუტენ-2; გ) ბუტენ-1? დაწერეთ შესაბამისი რეაქციების განტოლებები.
3. გაშიფრეთ გარდაქმნების შემდეგი ჯაჭვი. დაასახელეთ ნაერთები A, B, C. 4. შემოგვთავაზეთ 1-ქლოროპროპანიდან 2-ქლოროპროპანის მიღების მეთოდი. დაწერეთ შესაბამისი რეაქციების განტოლებები.
5. შემოგვთავაზეთ ეთილენის მინარევებისაგან ეთანის გაწმენდის მეთოდი. დაწერეთ შესაბამისი რეაქციების განტოლებები.
6. მოიყვანეთ რეაქციების მაგალითები, რომლებითაც შესაძლებელია გაჯერებული და უჯერი ნახშირწყალბადების გარჩევა.
7. 2,8 გ ალკენის სრული ჰიდროგენიზაციისთვის დაიხარჯა 0,896 ლიტრი წყალბადი (ნ.ე.). როგორია ამ ნაერთის მოლეკულური წონა და სტრუქტურული ფორმულა, რომელსაც აქვს ნახშირბადის ატომების ნორმალური ჯაჭვი?
8. რა აირი არის ბალონში (ეთენი თუ პროპენი), თუ ცნობილია, რომ ამ აირის 20 სმ3-ის სრული წვისთვის საჭიროა 90 სმ3 (ნ.ს.) ჟანგბადი?
9*. როდესაც ალკენი რეაგირებს ქლორთან სიბნელეში, წარმოიქმნება 25,4 გ დიქლორიდი, ხოლო როდესაც იგივე მასის ალკენი რეაგირებს ბრომთან ნახშირბადის ტეტრაქლორიდში, წარმოიქმნება 43,2 გ დიბრომიდი. განსაზღვრეთ საწყისი ალკენის ყველა შესაძლო სტრუქტურული ფორმულა.
აღმოჩენის ისტორია
ზემოაღნიშნული მასალიდან უკვე გავიგეთ, რომ ეთილენი არის უჯერი ნახშირწყალბადების ჰომოლოგიური სერიის წინაპარი, რომელსაც აქვს ერთი ორმაგი ბმა. მათი ფორმულა არის C n H 2n და მათ ალკენებს უწოდებენ.
1669 წელს გერმანელმა ექიმმა და ქიმიკოსმა ბეხერმა პირველმა მიიღო ეთილენი გოგირდმჟავას ეთილის სპირტთან რეაქციით. ბეჩერმა აღმოაჩინა, რომ ეთილენი ქიმიურად უფრო აქტიურია, ვიდრე მეთანი. მაგრამ, სამწუხაროდ, იმ დროს მეცნიერმა ვერ ამოიცნო წარმოქმნილი აირი და, შესაბამისად, მას არც ერთი სახელი არ დაუნიშნა.
ცოტა მოგვიანებით, ჰოლანდიელმა ქიმიკოსებმა იგივე მეთოდი გამოიყენეს ეთილენის წარმოებისთვის. და რადგან ქლორთან ურთიერთობისას იგი ცხიმოვან სითხეს ქმნიდა, შესაბამისად მიიღო სახელწოდება "ნავთობის გაზი". მოგვიანებით ცნობილი გახდა, რომ ეს სითხე იყო დიქლორეთანი.
ფრანგულად ტერმინი „ზეთი“ არის oléfiant. და მას შემდეგ, რაც ამ ტიპის სხვა ნახშირწყალბადები აღმოაჩინეს, ანტუან ფურკრუამ, ფრანგმა ქიმიკოსმა და მეცნიერმა, შემოიღო ახალი ტერმინი, რომელიც საერთო გახდა ოლეფინებისა და ალკენების მთელი კლასისთვის.
მაგრამ უკვე მეცხრამეტე საუკუნის დასაწყისში, ფრანგმა ქიმიკოსმა ჟ. გეი-ლუსაკმა აღმოაჩინა, რომ ეთანოლი შედგება არა მხოლოდ "ნავთობის" გაზისგან, არამედ წყლისგან. გარდა ამისა, იგივე აირი აღმოაჩინეს ეთილის ქლორიდში.
და მიუხედავად იმისა, რომ ქიმიკოსებმა დაადგინეს, რომ ეთილენი შედგება წყალბადისა და ნახშირბადისგან და უკვე იცოდნენ ნივთიერებების შემადგენლობა, მათ დიდი ხნის განმავლობაში ვერ იპოვნეს მისი ნამდვილი ფორმულა. და მხოლოდ 1862 წელს ე.ერლენმაიერმა მოახერხა ეთილენის მოლეკულაში ორმაგი ბმის არსებობის დამტკიცება. ეს ასევე აღიარა რუსმა მეცნიერმა ა.მ.ბუტლეროვმა და ექსპერიმენტულად დაადასტურა ამ თვალსაზრისის სისწორე.
ალკენების ბუნებაში გაჩენა და ფიზიოლოგიური როლი
ბევრ ადამიანს აინტერესებს კითხვა, სად შეიძლება ალკენების პოვნა ბუნებაში. ასე რომ, გამოდის, რომ ისინი პრაქტიკულად არ გვხვდება ბუნებაში, რადგან მისი უმარტივესი წარმომადგენელი, ეთილენი, არის მცენარეების ჰორმონი და მათში სინთეზირდება მხოლოდ მცირე რაოდენობით.
მართალია, ბუნებაში არსებობს ისეთი ალკენი, როგორიცაა მუსკალური. ეს ერთ-ერთი ბუნებრივი ალკენი არის ქალი სახლის ბუზის სექსუალური მიმზიდველი.
ყურადღება უნდა მიაქციოთ იმ ფაქტს, რომ მაღალი კონცენტრაციის მქონე ქვედა ალკენებს აქვთ ნარკოტიკული ეფექტი, რამაც შეიძლება გამოიწვიოს კრუნჩხვები და ლორწოვანი გარსების გაღიზიანება.
ალკენების გამოყენება
ძნელი წარმოსადგენია თანამედროვე საზოგადოების ცხოვრება პოლიმერული მასალების გამოყენების გარეშე. ვინაიდან, ბუნებრივი მასალისგან განსხვავებით, პოლიმერებს განსხვავებული თვისებები აქვთ, მათი დამუშავება მარტივია და ფასს თუ დავაკვირდებით, შედარებით იაფია. კიდევ ერთი მნიშვნელოვანი ასპექტი პოლიმერების სასარგებლოდ არის ის, რომ ბევრი მათგანი შეიძლება გადამუშავდეს.
ალკენებმა იპოვეს მათი გამოყენება პლასტმასის, რეზინის, ფილმების, ტეფლონის, ეთილის სპირტის, აცეტალდეჰიდის და სხვა ორგანული ნაერთების წარმოებაში.

სოფლის მეურნეობაში გამოიყენება, როგორც საშუალება, რომელიც აჩქარებს ნაყოფის დამწიფების პროცესს. პროპილენი და ბუტილენები გამოიყენება სხვადასხვა პოლიმერებისა და სპირტების წარმოებისთვის. მაგრამ სინთეზური რეზინის წარმოებაში გამოიყენება იზობუტილენი. აქედან გამომდინარე, შეგვიძლია დავასკვნათ, რომ შეუძლებელია ალკენების გარეშე, რადგან ისინი ყველაზე მნიშვნელოვანი ქიმიური ნედლეულია.
ეთილენის სამრეწველო გამოყენება
სამრეწველო მასშტაბით, პროპილენი ჩვეულებრივ გამოიყენება პოლიპროპილენის სინთეზისთვის და იზოპროპანოლის, გლიცეროლის, ბუტირალდეჰიდების და ა.შ. ყოველწლიურად იზრდება მოთხოვნა პროპილენზე.

4.3.ბ. წყალბადის ჰალოგენების დამატება (ჰიდროჰალოგენაცია)
კიდევ ერთი მნიშვნელოვანი ელექტროფილური დამატების რეაქცია ალკენებზე არის ალკენების დიდი ხნის ცნობილი ჰიდროჰალოგენაცია.
ქვემოთ მოცემულია HCl, HBr და HI დამატების ტიპიური მაგალითები სხვადასხვა ალკენებში.
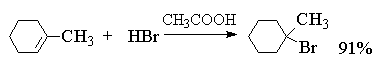

ალკილის შემცვლელების მოქმედება ორმაგ კავშირზე დამატების სიჩქარეზე აღწერილია შემდეგი თანმიმდევრობით:
R 2 C=CHR > RCH=CHR > RCH=CH 2
ეს შეესაბამება მექანიზმს, რომელშიც რეაქციის სიჩქარის განმსაზღვრელი საფეხური გულისხმობს კარბოკატიონის ფორმირებას, რადგან ალკილის კათიონების სტაბილურობა მცირდება რიგით მესამეული > მეორადი > პირველადი. ამრიგად, დამატების მექანიზმი უნდა მოიცავდეს ან თავისუფალი კარბოკაციური შუალედურის ფორმირებას, რომელიც იშვიათად შეინიშნება, ან შუალედური კარბოკაციონური ხასიათის. ბოლო შემთხვევა ყველაზე ტიპიურია.
თუ დამატება მოხდა „თავისუფალი კარბოკატიონის“ მეშვეობით, მაშინ რეაქცია იქნებოდა სრულიად არასტერეოსელექტიური, რადგან ალკილის კათიონებს აქვთ პლანშეტური სტრუქტურა. თუმცა, ჰიდროჰალოგენაცია, როგორც წესი, მიმდინარეობს სტერეოსელექტიურად და ალკენის სახეობიდან გამომდინარე, შერჩევითი ანტი- მიმაგრება, შერჩევითი სინ- ან შერეული სინ-ანტი- შეერთება.
ალკენებისთვის, რომლებშიც ორმაგი ბმა არ არის კონიუგირებული არომატულ რგოლთან, დამახასიათებელია ანტი- წყალბადის ჰალოგენის დამატება. ანტი- წყალბადის ქლორიდის და ბრომიდის, დეიტერიუმის ქლორიდის და ბრომიდის დამატება შეინიშნება ციკლოჰექსენისთვის, ციკლოპენტენისთვის, 1,2-დიმეთილჰექსენისთვის, 1,2-დიმეთილპენტენისთვის, ცის- და ტრანსი-ბუტენ-2, ჰექსენ-3 და მრავალი სხვა მარტივი ალკენი და ციკლოალკენი.
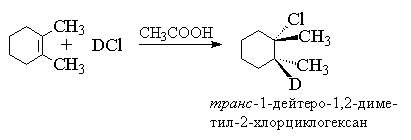
დამატებით პროდუქტში იდენტური შემცვლელები (მეთილის ჯგუფები) განლაგებულია ციკლოჰექსანის რგოლის შუა სიბრტყის სხვადასხვა მხარეს, ამიტომ იგი ეკუთვნის ტრანსი- რიგი. ანტი-დამატება ძნელია შეჯერდეს მექანიზმთან, რომელშიც ვარაუდობენ დისკრეტული კარბოკაციის წარმოქმნას. პლანარული კარბოკატიონისთვის, ჰალოგენური იონის მიერ ნუკლეოფილური შეტევა თანაბრად სავარაუდოა სიბრტყის ორივე მხარეს, რამაც უნდა გამოიწვიოს პროდუქტების ნარევის წარმოქმნა. სინ- და ანტი- შეერთებები. ალკენის ჰიდროჰალოგენიზაციის კინეტიკა ასევე მიუთითებს დამატების უფრო რთულ მექანიზმზე. არაკონიუგირებული ალკენებისთვის რეაქციის სიჩქარე აღწერილია მესამე რიგის განტოლებით მეორე რიგით წყალბადის ჰალოგენში, ანუ ის შეესაბამება Ad E 3 მექანიზმს.
v = k [ალკენი] 2
დამატების საწინააღმდეგო და მეორე რიგის რეაქცია წყალბადის ჰალოგენზე კარგად ეთანხმება Ad E 3 მექანიზმს, რომლის დროსაც ალკენი რეაგირებს წყალბადის ჰალოგენის ორ მოლეკულასთან, რომელთაგან ერთი მოქმედებს როგორც ელექტროფილური აგენტი, ხოლო მეორე, როგორც ნუკლეოფილური აგენტი.

ეს ტრიმოლეკულური მექანიზმი ვარაუდობს, რომ თავდაპირველად წარმოიქმნება ალკენის და ერთი წყალბადის ჰალოგენის მოლეკულის კომპლექსი, რასაც მოჰყვება მეორე HX მოლეკულის შეტევა ამ კომპლექსზე. ანტი- მხარეები დისკრეტული კარბოკატიონის წარმოქმნის გარეშე. განსაკუთრებით უნდა აღინიშნოს, რომ ნებისმიერი ტრიმოლეკულური მექანიზმი უნდა შედგებოდეს ორი თანმიმდევრული ეტაპისგან, რადგან სამი მოლეკულის ერთდროულად შეჯახება უკიდურესად ნაკლებად სავარაუდოა.

ანტი-დამატება მიუთითებს პრეფერენციულ ნუკლეოფილურ შეტევაზე წყალბადის ჰალოგენის მხრიდან იმ მხრიდან, სადაც ალკენი პროტონირებულია. წყალბადის ჰალოგენის ნაცვლად, ნუკლეოფილური აგენტის ფუნქცია ფინალურ ეტაპზე ასევე შეიძლება შეასრულოს ჰალოგენური იონმა. მართლაც, რეაქციის სიჩქარე ჩვეულებრივ იზრდება პირდაპირპროპორციულად ჰალოგენური იონის კონცენტრაციასთან, რომელიც შედის რეაქციულ ნარევში ტეტრაალკილამონიუმის ჰალოიდების NR 4+ X სახით. - ან ლითიუმის LiX. ამ შემთხვევაში, სტერეოსპეციფიკური ანტი- შეერთება.
ალკანებისთვის, რომლებშიც ორმაგი ბმული შერწყმულია არომატულ რგოლთან, დამახასიათებელია სინ- შეერთება ან შერეული სინ-ანტი- წყალბადის ჰალოგენის დამატება, მაგალითად:
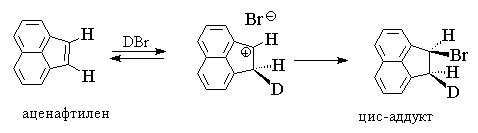
Syn დამატება არის დომინანტური პროცესი ცის- და ტრანსი-1-ფენილპროპენის, 1-ფენილ-4-ალკილციკლოჰექსენების, აცენაფთილენის, ინდენის იზომერები. როდესაც ასეთი ალკენები პროტონირებულია, წარმოიქმნება ბენზილის ტიპის კარბოკატები, რომლებიც უფრო სტაბილურია ვიდრე წმინდა ალკილის კათიონები, რომლებიც წარმოიქმნება ჩვეულებრივი ალკენების და ციკლოალკენების პროტონაციის დროს. რეაქციის კინეტიკა ამ შემთხვევაში ჩვეულებრივ აღწერილია უფრო მარტივი მეორე რიგის განტოლებით v = k[ალკენი], ანუ ის შეესაბამება ბიმოლეკულურ Ad E 2 მექანიზმს. Ad E 2-მექანიკა გულისხმობს იონური წყვილის წარმოქმნას, რომელიც მოიცავს კარბოკატიონსა და ჰალოგენურ იონს.

დამატების მექანიზმი, რომელიც მოიცავს იონურ წყვილებს, არ შეიძლება იყოს ძალიან სტერეოელექტიური. თუ იონური წყვილი საბოლოო პროდუქტად გარდაიქმნება უფრო სწრაფად, ვიდრე მას შეუძლია ბრუნოს ერთი ნახშირბად-ნახშირბადის ბმის გარშემო, საბოლოო შედეგი იქნება სინ- დამატება, სადაც პროტონი და ჰალოგენური იონი ემატება ორმაგი ბმის ერთ მხარეს. წინააღმდეგ შემთხვევაში, ისეთი პროდუქტების ფორმირება, როგორიცაა სინ- ისე ანტი- NH-ის კავშირი. ეს შემთხვევა ხდება ჰიდროჰალოგენაციის დროს წყვილი-ჩანაცვლებული სტირონი Z-C6H4-CH=CH2. აქ დაფიქსირებული ნიმუში არის ის სინ- დანამატი დამახასიათებელია მხოლოდ იმ ოლეფინებისთვის, რომლებიც პროტონიზაციისას იძლევა შედარებით სტაბილურ კარბოკატიონს, ანუ დონორი შემცვლელების შემთხვევაში Z.
ჰიდროჰალოგენაციის რეაქციები, რომლებიც მიმდინარეობს Ad E 2 მექანიზმით, ხასიათდება კონიუგატის დამატებისა და გადაწყობის პროცესებს შორის კონკურენციით, ვინაიდან შუალედში წარმოიქმნება კარბოკატიონი ან იონური წყვილი.

როგორც ალკილის ჯგუფის და ჰიდრიდის იონის 1,2-მიგრაციით გადაწყობის მაგალითი, წარმოგიდგენთ ტერტ-ბუტილეთილენის და იზოპროპილეთილენის ჰიდროჰალოგენაციის რეაქციებს, შესაბამისად.

როდესაც იგივე რეაქცია ტარდება გამხსნელის გარეშე ცივში (-78 0 C), წარმოიქმნება 33% ნორმალური და 67% არანორმალური (გადაჯგუფებული) დანამატის პროდუქტების ნარევი.

4.3.გ. ორიენტაცია. მარკოვნიკოვის წესი
სიმეტრიული ელექტროფილებისგან განსხვავებით (Hal 2), წყალბადის ჰალოგენები არასიმეტრიული ელექტროფილური რეაგენტებია. ნებისმიერი არასიმეტრიული ელექტროფილის (HBr, ICl, H2O, Hg(OAc)2 და ა.შ.) დამატება არასიმეტრიულ ალკენში, პრინციპში, შეიძლება წარმოქმნას ორი ალტერნატიული პროდუქტის ნარევი, მაგრამ პრაქტიკაში მხოლოდ ერთი მათგანი ყალიბდება. მაგალითად, განვიხილოთ წყალბადის ბრომიდის დამატება პროპილენში.

ჯერ კიდევ 1870 წელს ვ.ვ. მარკოვნიკოვმა ჩამოაყალიბა ემპირიული წესი, რომლის მიხედვითაც არასიმეტრიული ალკენები ამატებენ HX-ს ისე, რომ უპირატესად წარმოიქმნება პროდუქტი, რომელშიც წყალბადს ემატება ორმაგი ბმის ყველაზე ნაკლებად ჩანაცვლებული ბოლო, X-ს კი ყველაზე ჩანაცვლებული ბოლო.
მარკოვნიკოვის წესი, როგორც წესი, აიხსნება ორი ალტერნატიული კარბოკაციონის სტაბილურობის სხვაობით. მაგალითად, ზემოთ მოცემულ მაგალითში ნორმალურია ნ-პროპილის კატიონი გაცილებით ნაკლებად სტაბილურია, ვიდრე იზოპროპილის კატიონი და, შესაბამისად, რეაქცია მიმდინარეობს მეორე გზაზე.
მარკოვნიკოვის წესი თავდაპირველად გამოიყენებოდა მხოლოდ HX-ის ნახშირწყალბადების სუბსტრატებში დამატების შემთხვევაში, მაგრამ პრინციპში ის შეიძლება გავრცელდეს სხვა ჩანაცვლებული ალკენების რეაქციებზე. ამრიგად, HCl-ის დამატება CF 3 CH=CH 2-ში იძლევა " ანტი-მარკოვნიკოვის" პროდუქტი CF 3 CH 2 CH 2 Cl. ეს მოსალოდნელი იყო, რადგან CF 3 CH + CH 3 კატიონი ნაკლებად სტაბილურია ვიდრე CF 3 CH 2 CH 2 + კატიონი ძლიერი (-I) ეფექტის გამო. CF 3 ჯგუფი უპირატესად წარმოიქმნება კატიონი CF 3 CH 2 CH 2 +, მაგრამ ის ასევე, თუმცა ნაკლებად დესტაბილიზებულია CF 3 ჯგუფის ინდუქციური ეფექტით, რის შედეგადაც HCl-ის დამატება ხდება ტრიფტორმეთილენში. გაცილებით ნელა ვიდრე შეუცვლელი ეთილენის დამატება.
მსგავსი მიზეზის გამო, ვინილის ტრიალკილამონიუმის კათიონები ამატებენ HBr-ს ასევე მარკოვნიკოვის წესის საწინააღმდეგოდ:
HX-ის დამატება ძლიერი (-I) და (-M) შემცვლელების მქონე ალკენებში, მაგალითად, აკრილონიტრილში ან ნიტროეთილენში, ასევე უნდა ეწინააღმდეგებოდეს მარკოვნიკოვის წესს. თუმცა, ამ შემთხვევაში, ორმაგი ბმა იმდენად ძლიერად დეაქტივირებულია ელექტროფილურ რეაგენტებთან მიმართებაში, რომ ეს რეაქციები ხდება მხოლოდ ძალიან მკაცრ პირობებში. ვინილის ქლორიდი CH 2 =CHCl ყოველთვის იძლევა ექსკლუზიურად „მარკოვნიკოვის დანამატებს“. მაგალითად, როდესაც ის რეაგირებს HCl-თან, წარმოიქმნება მხოლოდ 1,1-დიქლოროეთანი (გემინალური დიქლორიდი) CH 3 CHCl 2. ქლორს, CF 3 ჯგუფის მსგავსად, აქვს ძლიერი (-I) ეფექტი და ერთი შეხედვით ჩანს, რომ ამ მიზეზით დანამატს უნდა ჰქონდეს ანტიმარკოვნიკოვის ორიენტაცია, ვინაიდან + CH 2 CH 2 Cl კატიონი უნდა იყოს უფრო სტაბილური ვიდრე კათიონი CH 3 CH + Cl. თუმცა, CF 3 ჯგუფისგან განსხვავებით, ქლორს, გარდა (-I) ეფექტისა, აქვს საწინააღმდეგო (+M) ეფექტიც (რადგან მას აქვს მარტოხელა წყვილი). გამოცდილება გვიჩვენებს, რომ მეზომერული ეფექტის სიდიდე სავსებით საკმარისია 1-ქლოროეთილის კატიონის ენერგიის დასაწევად 2-ქლოროეთილის კატიონის ენერგეტიკული დონის ქვემოთ, რომელშიც +M ეფექტი არ ვლინდება.
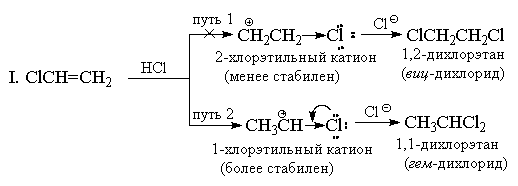
II. რეზონანსული თეორიის თვალსაზრისით, 1-ქლოროეთილის კატიონის სტრუქტურა შეიძლება წარმოდგენილი იყოს შემდეგნაირად:
თუმცა, ვინილის ქლორიდის დამატება ხდება უფრო ნელა, ვიდრე ეთილენში იმავე პირობებში, ანუ, მთლიანი ეფექტის მიხედვით (-I > +M), ქლორი რჩება ელექტრონის შემცვლელად წყალბადთან და 1-ქლოროეთილის კატიონთან შედარებით. ნაკლებად სტაბილურია, ვიდრე C 2 H 5 + . სხვა ვინილის ჰალოიდები ანალოგიურად რეაგირებენ HX-თან.
ვინილის ეთერები CH 2 =CHOR დაამატეთ HX (X=Hal) მარკოვნიკოვის წესის მიხედვით ბევრად უფრო მაღალი სიჩქარით, ვიდრე ზემოთ ჩამოთვლილი ყველა ჩანაცვლებული ალკენი. ეს განპირობებულია RO ჯგუფის მნიშვნელოვანი +M ეფექტით. ქლორის ატომისგან განსხვავებით, RO ჯგუფი, მთლიანი ელექტრონული ეფექტის თვალსაზრისით (+M > -I), არის ძლიერი ელექტრონის შემომტანი შემცვლელი, რომელიც ეფექტურად ასტაბილურებს მეზობელ კარბოკაციურ ცენტრს. კარბოკატიონის სტრუქტურა ამ შემთხვევაში ასევე შეიძლება წარმოდგენილი იყოს როგორც ორი რეზონანსული სტრუქტურის ნაკრები
ჰალოგენური ანიონის მიერ ოქსონიუმის კატიონის შეტევა იწვევს CH 3 CH(Hal)OR ტიპის α-ჰალოგენური ეთერების წარმოქმნას.
4.3.გ. ალკენების დატენიანება
ალკენების მჟავით კატალიზებული დატენიანება იწვევს ალკოჰოლების წარმოქმნას. ალკენების დატენიანების მიმართულება განისაზღვრება მარკოვნიკოვის წესით, ამიტომ ვარაუდობენ, რომ ამ რეაქციაში შუალედური ნაწილაკის სახით წარმოიქმნება კარბოკატიონი.
მეორადი ალკილის კარბოკაციონების გადაწყობის ტენდენცია ხელს უშლის ალკენების ჰიდრატაციის გამოყენებას მეორადი სპირტების წარმოებისთვის.

ამ მეთოდმა იპოვა შეზღუდული გამოყენება ლაბორატორიაში მხოლოდ მესამეული სპირტების დასამზადებლად. ჰიდრატაციის რეაქცია ამ შემთხვევაში დიდწილად შექცევადია და მესამეული სპირტები წარმოიქმნება დაბალი მოსავლიანობით (40-45%).
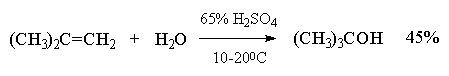

უმარტივესი ალკენების - ეთილენისა და პროპილენის ჰიდრატაცია მნიშვნელოვანი სამრეწველო მეთოდია ეთილის და იზოპროპილის სპირტების წარმოებისთვის.

ლაბორატორიულ პრაქტიკაში, ალკენების პირდაპირ დატენიანებას არ ჰპოვა ფართო გამოყენება, როგორც მკაცრი პირობების, ისე იზომერული სპირტების მნიშვნელოვანი რაოდენობით წარმოქმნის გამო. ამჟამად, ჰიდროქსიმერკურაციის დაკავშირებული რეაქცია - დემერკურაცია - ჩვეულებრივ გამოიყენება ალკენებიდან ალკოჰოლების რეგიოსელექტიური წარმოებისთვის.
4.3.დ. ჰიდროქსიმერკურაცია-დემერკურაცია
ალკენის ორმაგ ბმაზე ელექტროფილური შეტევა შეიძლება განხორციელდეს ლითონის იონების მიერ, რომელთა შორის განსაკუთრებული პოზიცია იკავებს ვერცხლისწყლის(II) კატიონს. ვერცხლისწყლის აცეტატი ძალიან რბილ პირობებში 20 0C ტემპერატურაზე ემატება ალკენებს წყალში ტეტრაჰიდროფურანში (THF) ან წყალმჟავას წყალმჟავას ვერცხლისწყლის ორგანოების ნაერთების წარმოქმნით. ვერცხლისწყლის აცეტატის დამატება ორმაგ კავშირში რეგიოსპეციფიკურად მიმდინარეობს მარკოვნიკოვის წესის მკაცრი დაცვით, ანუ ვერცხლისწყლის კატიონი მიმაგრებულია ყველაზე ნაკლებად შემცვლელ ნახშირბადის ატომზე.
C-Hg ბმა ორგანულ ვერცხლისწყალ ნაერთებში შეიძლება ადვილად დაიშალოს ნატრიუმის ბოროჰიდრიდის NaBH 4 მოქმედებით, წარმოიქმნება ვერცხლისწყალი და ახალი C-H ბმა. ვარაუდობენ, რომ ალკილმერკური ჰიდრიდი მიიღება როგორც არასტაბილური შუალედი, რომელიც შემდგომ იშლება და რადიკალური მექანიზმით გამოიყოფა მეტალის ვერცხლისწყალი.

მთლიანობაში, ჰიდროქსიმერკურაცია-დემერკურაციის ეს ორეტაპიანი პროცესი საბოლოოდ წარმოადგენს ალკენის რეგიოსპეციფიკურ ჰიდრატაციას მარკოვნიკოვის წესის მიხედვით უკიდურესად რბილ პირობებში, როდესაც ქვეპროდუქტების წარმოქმნა შემცირებულია მაქსიმალურ მინიმუმამდე. ამის ნათლად ილუსტრაცია შესაძლებელია შემდეგი მაგალითების გამოყენებით, რომლებშიც რეაქციის პროდუქტების მთლიანი გამოსავლიანობა არის 90-98%. მოცემული ციფრული მონაცემები ამ შემთხვევაში არ მიუთითებს მიღებული ნაერთების მოსავლიანობაზე, არამედ მათ თანაფარდობაზე ნარევში.




როგორც ზემოაღნიშნული მაგალითებიდან ჩანს, ალკენების ჰიდროქსიმერკურაცია-დემერკურაცია უმეტეს შემთხვევაში უზრუნველყოფს ალკენების რეგიოსპეციფიკურ დატენიანებას ორი იზომერული სპირტიდან თითქმის მხოლოდ ერთის წარმოქმნით. აღსანიშნავია, რომ არ არის საჭირო ორგანომერკური ნაერთის იზოლირება და ორივე პროცესი შეიძლება განხორციელდეს უშუალოდ ერთმანეთის მიყოლებით.
უსიმეტრიული ალკენების ჰიდროქსიმერკურაცია, როგორც ჩანს, იწყება AcOHg + კატიონის შეტევით და არასიმეტრიული ციკლური ვერცხლისწყლის კატიონის (არასიმეტრიული ჰალოგენიუმის იონის ანალოგი) შუალედური წარმოქმნით, რომელიც შემდეგ იხსნება წყლის ბირთვული შეტევის შედეგად. ჩანაცვლებული ნახშირბადის ატომი, რომელიც ატარებს უფრო დიდ დადებით მუხტს.

შემაერთებელი ვერცხლისწყლის იონი შეიძლება დაფიქსირდეს არანუკლეოფილურ ძლიერ მჟავე გარემოში, თუნდაც 20 0 C ტემპერატურაზე უფრო ძლიერი ელექტროფილური აგენტის - ვერცხლისწყლის ტრიფტორაცეტატის დამატებით ფტორსულფონის მჟავისა და ანტიმონის პენტაფტორიდის ნარევში.

ვერცხლისწყლის კატიონი შეიძლება დაიშალოს არა მხოლოდ წყლის მოქმედებით, არამედ სხვა ელექტრონების შემომწირველი გამხსნელებით: სპირტები, ძმარმჟავა, აცეტონიტრილი და ა.შ. რეაქციის საბოლოო პროდუქტი ამ შემთხვევაში იქნება ეთერები, აცეტატები ან N-შემცვლელი ამიდები. ძმარმჟავა, შესაბამისად, მაგალითად:


როდესაც განშტოებული მეორადი ან მესამეული სპირტები გამოიყენება ალკოქსიმერკურაცია-დემერკურაციის რეაქციაში, ტრიფტორაცეტატი Hg (OCOCF 3) 2 ან ვერცხლისწყლის ტრიფლატი Hg (OSO 2 CF 3) 2 უფრო ეფექტურია, ვიდრე ვერცხლისწყლის აცეტატი.

ამრიგად, ჰიდროქსი- და ალკოქსიმერკურაცია-დემერკურაცია არის ერთ-ერთი საუკეთესო მოსამზადებელი მეთოდი ალკოჰოლებისა და ეთერების სინთეზისთვის განშტოებული ალკილის რადიკალებით.
ვერცხლისწყლის მარილების დამატება ალკენებში არის ორმაგი ბმის კონიუგირებული დამატების რეაქციის ყველაზე ნათელი მაგალითი, სადაც გარე ნუკლეოფილური აგენტის როლს ასრულებს გამხსნელი. ორმაგი ჰიდროქსიმერკურაცია-დემერკურაციის პროცესის სტერეოქიმია დამოკიდებულია თითოეული ინდივიდუალური ნაბიჯის სტერეოქიმიურ შედეგზე. ჰიდროქსიმერკურაციას ახასიათებს ანტი- დამატება, როგორც სხვა რეაქციებს, რომლებიც მოიცავს ციკლურ კატიონს. თუმცა, რადიკალური დემერკურაცია არ არის ძალიან სტერეოელექტიური. მაშასადამე, მთელი პროცესი მთლიანობაში ასევე არასტერეოსპეციფიკურია.
4.3.ე. ალკენების დამატება (კათიონური დიმერიზაცია და ალკენების პოლიმერიზაცია)
ამ ტიპის რეაქციის ყველაზე საინტერესო მაგალითია იზობუტილენის დიმერიზაცია და პოლიმერიზაცია გოგირდმჟავას თანდასწრებით.

ალკენების ამ ნარევის ტექნიკური სახელწოდებაა "დიიზობუტილენი". ეს რეაქცია მიმდინარეობს კათიონური მექანიზმით, ალკენების ორმაგ ბმაში მინერალური მჟავების დამატების მექანიზმის მსგავსი. პირველ ეტაპზე პროტონი მიმაგრებულია იზობუტილენის მოლეკულასთან შედარებით სტაბილურად რუბლს შეადგენს-ბუტილის კატიონი. შემდგომ ჩამოყალიბდა რუბლს შეადგენს-ბუტილის კატიონი (ლუისის მჟავა) რეაგირებს იზობუტილენის მოლეკულასთან (ლუისის ბაზა) ახალი სტაბილური მესამეული ოქტილის კატიონის წარმოქმნით.

ამ პირობებში, ფუძეების მოქმედებით (H 2 O, HSO 4 - იონები), ოქტილის კარბოკატიონი სწრაფად კარგავს პროტონს და იქცევა იზომერული პენტენების ნარევში, რადგან პროტონის აბსტრაქცია ხდება ორი განსხვავებული პოზიციიდან:

თერმოდინამიკურად ნაკლებად სტაბილური ალკენის - 2,4,4-ტრიმეთილპენტენ-1 (80% რეაქციულ ნარევში) შეღავათიანი ფორმირება დაკავშირებულია მეთილის ჯგუფების წყალბადის ატომების ფუძის შეტევის უფრო დიდ სივრცით ხელმისაწვდომობასთან შედარებით წყალბადთან შედარებით. მეთილენის ჯგუფის ატომები. ინდუსტრიაში, "დიიზობუტილენი" ჰიდროგენირებულია Ni-Raney-ით, რათა წარმოიქმნას "იზოოქტანი" (ნახშირწყალბადის 2,2,4-ტრიმეთილპენტანის ტექნიკური სახელი), რომელიც გამოიყენება როგორც მაღალი ოქტანის საწვავი შიდა წვის ძრავებისთვის.
გოგირდმჟავას მაღალი კონცენტრაციის დროს (80%-ზე მეტი), იზობუტილენის კათიონური პოლიმერიზაცია ხდება პოლიმერის წარმოქმნით, რომელსაც ეწოდება პოლიიზობუტილენი (-CH 2 C(CH 3) 2 -) n. ეს რეზინისმაგვარი პოლიმერი გამოიყენება ანტიკოროზიული და ჰიდროსაიზოლაციო საფარის, დალუქვის და ა.შ.
იზობუტილენის გარდა, კათიონური მექანიზმით პოლიმერიზებულია 3-მეთილბუტენ-1, ვინილის ეთერები და სტიროლის ზოგიერთი წარმოებული, რომელსაც შეუძლია შედარებით სტაბილური კარბოკაციების წარმოქმნა. წყალბადის ფტორი და ლუისის მჟავები ასევე გამოიყენება კათიონური პოლიმერიზაციის კატალიზატორებად: BF 3, AlCl 3, AlBr 3 და ა.შ. ძალიან მცირე რაოდენობით წყლის თანდასწრებით.
4.3.გ. ალკანების დამატება (ალკენების ალკილაცია)
"იზოოქტანის" სინთეზის კიდევ ერთი სამრეწველო მეთოდი ემყარება იზობუტილენის რეაქციას ჭარბი იზობუტანთან კონცენტრირებული გოგირდმჟავას თანდასწრებით ან უწყლო წყალბადის ფტორში 0 10 0 C ტემპერატურაზე.

ეს რეაქციაც კატიონური მექანიზმით მიმდინარეობს და რაც განსაკუთრებით საინტერესოა ჯაჭვური კათიონური პროცესის მაგალითია. პირველი, იზობუტილენი დიმერიზდება რეაქციის პირობებში, რათა წარმოქმნას მესამეული ოქტილის კატიონი (CH 3) 3 CCH 2 C + (CH 3) 2. მისი ფორმირების მექანიზმი დეტალურად არის აღწერილი წინა ნაწილში. შემდეგ ხდება წყალბადის სწრაფი გადატანა (ჰიდრიდის იონის სახით) იზობუტანიდან ოქტილ კატიონში „იზოოქტანის“ მოლეკულისა და ახალი ტერტ-ბუტილის კატიონის წარმოქმნით, რომელიც თავის მხრივ სწრაფად რეაგირებს იზობუტილენთან და ქმნის ახალს. ოქტილის კატიონი და ა.შ.
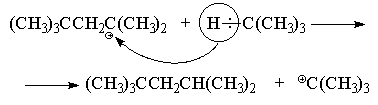
"იზოოქტანის" სინთეზის გარდა, ეს ალკილაციის მეთოდი გამოიყენება ნავთობქიმიურ ინდუსტრიაში მაღალი დუღილის განშტოებული ნახშირწყალბადების სინთეზისთვის განშტოებული ალკენებიდან და დაბალი დუღილის ალკანებიდან თერმული კრეკინგის ფრაქციის გამოყენებით.
ალკენები
ნახშირწყალბადები, რომელთა მოლეკულაში ნახშირბად-ნახშირბადის და ნახშირბად-წყალბადის მარტივი σ-ბმების გარდა არის ნახშირბად-ნახშირბადის π-ბმები, ე.წ. შეუზღუდავი.ვინაიდან π ბმის წარმოქმნა ფორმალურად ექვივალენტურია მოლეკულის მიერ წყალბადის ორი ატომის დაკარგვასთან, უჯერი ნახშირწყალბადები შეიცავს 2გვწყალბადის ატომები ნაკლებია, ვიდრე შემზღუდველი, სადაც P -π ობლიგაციების რაოდენობა:
სერია, რომლის წევრები განსხვავდებიან ერთმანეთისგან (2H) n-ით, ეწოდება იზოლოგიური სერია.ამრიგად, ზემოხსენებულ სქემაში იზოლოგებია ჰექსანები, ჰექსენები, ჰექსადიენები, ჰექსინები, ჰექსატრიენები და ა.შ.
ნახშირწყალბადებს, რომლებიც შეიცავს ერთ π ბმას (ანუ ორმაგ ბმას) უწოდებენ ალკენები (ოლეფინები)ან სერიის პირველი წევრის - ეთილენის მიხედვით, ეთილენის ნახშირწყალბადები.მათი ჰომოლოგიური სერიის ზოგადი ფორმულა არის C p H 2l.
1. ნომენკლატურა
IUPAC-ის წესების შესაბამისად, ალკენების სახელების აგებისას, ყველაზე გრძელ ნახშირბადის ჯაჭვს, რომელიც შეიცავს ორმაგ ბმას, ენიჭება შესაბამისი ალკანის სახელი, რომელშიც დასასრული -ანშეცვალა -en.ეს ჯაჭვი დანომრილია ისე, რომ ნახშირბადის ატომები, რომლებიც მონაწილეობენ ორმაგი ბმის ფორმირებაში, იღებენ ყველაზე დაბალ რიცხვებს:

რადიკალებს ასახელებენ და ითვლიან, როგორც ალკანების შემთხვევაში.
შედარებით მარტივი სტრუქტურის ალკენებისთვის დასაშვებია უფრო მარტივი სახელები. ამრიგად, ზოგიერთი ყველაზე ხშირად წარმოქმნილი ალკენი დასახელებულია სუფიქსის დამატებით -enნახშირწყალბადის რადიკალის სახელით იგივე ნახშირბადის ჩონჩხით:
ალკენებისგან წარმოქმნილი ნახშირწყალბადის რადიკალები იღებენ სუფიქსს -ენილი.რადიკალში ნუმერაცია იწყება ნახშირბადის ატომიდან, რომელსაც აქვს თავისუფალი ვალენტობა. ამასთან, უმარტივესი ალკენილის რადიკალებისთვის, სისტემატური სახელების ნაცვლად, ნებადართულია ტრივიალურის გამოყენება:

წყალბადის ატომებს, რომლებიც უშუალოდ უკავშირდება ნახშირბადის უჯერი ატომებს, რომლებიც ქმნიან ორმაგ კავშირს, ხშირად უწოდებენ ვინილის წყალბადის ატომები,
2. იზომერიზმი
ნახშირბადის ჩონჩხის იზომერიზმის გარდა, ორმაგი ბმის პოზიციის იზომერიზმი ასევე ვლინდება ალკენების სერიაში. ზოგადად, ამ ტიპის იზომერიზმი არის შემცვლელის პოზიციის (ფუნქციის) იზომერიზმი- შეინიშნება ყველა შემთხვევაში, როდესაც მოლეკულა შეიცავს რაიმე ფუნქციურ ჯგუფს. ალკანისთვის C4H10 შესაძლებელია ორი სტრუქტურული იზომერი:
C4H8 ალკენისთვის (ბუტენი) შესაძლებელია სამი იზომერი:

ბუტენ-1 და ბუტენ-2 არის ფუნქციის პოზიციის იზომერები (ამ შემთხვევაში მის როლს ასრულებს ორმაგი ბმა).
სივრცითი იზომერები განსხვავდებიან შემცვლელების სივრცითი განლაგებით ერთმანეთთან შედარებით და ე.წ. cis იზომერები,თუ შემცვლელები განლაგებულია ორმაგი ბმის იმავე მხარეს და ტრანს იზომერები,თუ მოპირდაპირე მხარეს:

3. ორმაგი ბმის სტრუქტურა
მოლეკულის გაყოფის ენერგია C=C ორმაგ ბმაზე არის 611 კჯ/მოლი; ვინაიდან C-C σ ბმის ენერგია არის 339 კჯ/მოლი, π ბმის გაწყვეტის ენერგია არის მხოლოდ 611-339 = 272 კჯ/მოლი. π -ელექტრონები გაცილებით მსუბუქია, ვიდრე σ -ელექტრონები და მგრძნობიარეა, მაგალითად, პოლარიზებული გამხსნელების ან ნებისმიერი შემტევი რეაგენტის გავლენის მიმართ. ეს აიხსნება σ- და π-ელექტრონების ელექტრონული ღრუბლის განაწილების სიმეტრიის სხვაობით. p-ორბიტალების მაქსიმალური გადაფარვა და, შესაბამისად, მოლეკულის მინიმალური თავისუფალი ენერგია რეალიზებულია მხოლოდ ვინილის ფრაგმენტის ბრტყელი სტრუქტურით და შემცირებული C-C მანძილით, რომელიც ტოლია 0,134 ნმ, ე.ი. მნიშვნელოვნად ნაკლებია მანძილი ნახშირბადის ატომებს შორის, რომლებიც დაკავშირებულია ერთი ბმით (0,154 ნმ). როდესაც მოლეკულის "ნახევრები" ბრუნავს ერთმანეთთან შედარებით ორმაგი ბმის ღერძის გასწვრივ, ორბიტალური გადახურვის ხარისხი მცირდება, რაც დაკავშირებულია ენერგიის მოხმარებასთან. ამის შედეგია ორმაგი ბმის ღერძის გასწვრივ თავისუფალი ბრუნვის არარსებობა და ნახშირბადის ატომებში შესაბამისი ჩანაცვლებით გეომეტრიული იზომერების არსებობა.
ალკენები- უჯერი ნახშირწყალბადები, რომლებიც შეიცავს ერთ ორმაგ კავშირს. ალკენების მაგალითები:

ალკენების მიღების მეთოდები.
1. ალკანების კრეკინგი 400-700°C-ზე. რეაქცია ხდება თავისუფალი რადიკალების მექანიზმით:

2. ალკანების დეჰიდროგენაცია:
3. ელიმინაციის რეაქცია (ელიმინაცია): მეზობელი ნახშირბადის ატომებიდან გამოიყოფა 2 ატომი ან ატომების 2 ჯგუფი და წარმოიქმნება ორმაგი ბმა. ასეთი რეაქციები მოიცავს:
ა) ალკოჰოლური სასმელების გაუწყლოება (150°C-ზე ზევით გათბობა, გოგირდმჟავას, როგორც წყლის გამწმენდი რეაგენტის მონაწილეობით):
ბ) წყალბადის ჰალოიდების ელიმინაცია ტუტე ალკოჰოლური ხსნარის ზემოქმედებისას:

წყალბადის ატომი უპირატესად გამოიყოფა ნახშირბადის ატომისგან, რომელიც დაკავშირებულია წყალბადის ნაკლებ ატომებთან (ყველაზე ნაკლებად წყალბადირებული ატომი) - ზაიცევის მმართველობა.
ბ) დეჰალოგენაცია:

ალკენების ქიმიური თვისებები.
ალკენების თვისებები განისაზღვრება მრავალჯერადი ბმის არსებობით, ამიტომ ალკენები შედიან ელექტროფილურ დამატების რეაქციებში, რომლებიც ხდება რამდენიმე ეტაპად (H-X - რეაგენტი):
1 ეტაპი:

მე-2 ეტაპი:
 .
.
ამ ტიპის რეაქციაში წყალბადის იონი მიეკუთვნება ნახშირბადის ატომს, რომელსაც აქვს უფრო უარყოფითი მუხტი. სიმკვრივის განაწილება არის:

თუ შემცვლელი არის დონორი, რომელიც ავლენს +I- ეფექტს, მაშინ ელექტრონის სიმკვრივე გადადის ყველაზე ჰიდროგენირებული ნახშირბადის ატომისკენ, რაც მასზე ნაწილობრივ უარყოფით მუხტს ქმნის. რეაქციები მიმდინარეობს შესაბამისად მარკოვნიკოვის წესი: პოლარული მოლეკულების შეერთებისას მოსწონს NH (HCl, HCN, ჰოჰა.შ.) არასიმეტრიულ ალკენებს წყალბადი უპირატესად ემაგრება ორმაგ ბმაზე უფრო ჰიდროგენიზებულ ნახშირბადის ატომს.
ა) დანამატის რეაქციები:
1) ჰიდროჰალოგენაცია:
რეაქცია მარკოვნიკოვის წესს მოჰყვება. მაგრამ თუ პეროქსიდი იმყოფება რეაქციაში, მაშინ წესი არ არის გათვალისწინებული:
2) დატენიანება. რეაქცია მიჰყვება მარკოვნიკოვის წესს ფოსფორის ან გოგირდმჟავას თანდასწრებით:

3) ჰალოგენაცია. შედეგად, ბრომის წყალი უფერულდება - ეს არის თვისებრივი რეაქცია მრავალჯერადი ბმაზე:
4) ჰიდროგენიზაცია. რეაქცია ხდება კატალიზატორების თანდასწრებით.



